1. Erste Schritte und Musterfragen
Eizellspende ist in Deutschland und in der Schweiz verboten, in Österreich kaum verfügbar.
Es gibt jedoch Länder, die die anonyme oder die offene Spende von Eizellen zulassen.
Hat man sich für eine Klinik dort entschieden gilt: Ein Erstgespräch ist noch kein Behandlungsvertrag. Entscheidet sich das Paar dagegen, entstehen für das Erstgespräch einige hundert Euro Beratungskosten.
Es ist hilfreich, aber nicht zwingend notwendig, Befunde und Unterlagen der eignen homologen Behandlungen mitzubringen. Wichtig sind folgende Fragen:
- Hat sich die Schleimhaut immer regelrecht aufgebaut?
- Gibt es Myome oder andere Probleme in der Gebärmutter?
- Sind ausreichend Spermien für eine ICSI vorhanden?
Wenn wir uns dafür entscheiden: wie ist dann der Ablauf?
Voran steht eine umfassende Internetrecherche über die Kliniken. Im zweiten Schritt folgt die Kontaktaufnahme per Email mit detaillierten Musterfragen.
Durch mehrere Anfragen bei IVF-Zentren erhält man auf diese Weise eine Basis für die Entscheidung. Hilfreich ist, wenn ein Videotelefonat mit dem Arzt / der Ärztin angeboten wird.
Download Musterfragen
Was passiert im Erstgespräch?
Zum Schluss sollte man ein bis maximal zwei seiner persönlichen Favoriten aufsuchen, um dort das Erstgespräch vor Ort zu führen. Ein Erstgespräch beinhaltet folgende Bausteine:
- Umfassende Information über die Behandlung , Chancen und Risiken
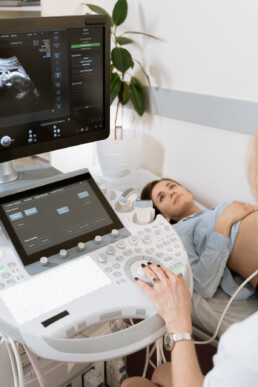
- Ultraschall und evtl. Blutabnahme bei der Frau
- Kryokonservierung des Spermas des Mannes
- Unterzeichnung der Behandlungsverträge
- Aushändigung der Medikamente bzw. Rezeptausstellung für die Empfängerin
- Ausstellung eines Behandlungsplanes
- Festlegung eines Zeitpunktes der Behandlung.
Viele Zentren bieten im Erstgespräch eine möglichst komplette Abwicklung inklusive Kryokonservierung der abgegebenen Spermaprobe und Aushändigung der Medikamente für die Empfängerin an. Eine Anreise der Empfängerin ist anschließend nur zum Embryonentransfer notwendig. Abstimmungen zwischendurch und insbesondere die Festlegung von Tag 1 der Behandlung erfolgen telefonisch oder per Email.
Eine zentrale Stellung nimmt die Patientenkoordinatorin ein. Sie ist sehr gut ausgebildet, spricht deutsch und hat einen direkten Kontakt zum Arzt bzw. zur Ärztin.
„Ich befürworte ein Erstgespräch vor Ort, da bei einem Videocall kein Gesamteindruck von Größenordnung, Räumlichkeiten, Team und Atmosphäre entsteht. Videocall kann vorausgehen. Zudem kann beim Erstgespräch in der Klinik bereits das Sperma des Mannes eingefroren werden. Somit reicht später die Anreise zum Embryonentransfer.“
– Christine Büchl
Die Behandlung der Spenderin
Im frischen Behandlungszyklus selbst gibt es zwei Patientinnen: die Spenderin und die Empfängerin. Beide brauchen jeweils einen optimalen Zeitpunkt für die Eizellentnahme bzw. für den Embryonentransfer. Oberstes Ziel für die Spenderin ist, dass ihre Behandlung möglichst nebenwirkungsarm erfolgt. Oberstes Ziel für die Empfängerin ist, zum richtigen Zeitpunkt empfängnisbereit zu sein.
Im frischen Zyklus wartet die Empfängerin auf die Spenderin, denn die Empfängerin kann ca. zwei bis drei Wochen „empfängnisbereit“ gehalten werden. Irgendwann in diesem Zeitraum fällt die Punktion der Spenderin und das fünftägige Programm des Embryos im IVF-Labor beginnt. Ob der Embryonentransfer jetzt am Zyklustag 18 oder 27 der Empfängerin stattfindet, spielt dabei keine Rolle. Entscheidend ist einzig und allein, dass der Eintritt der Empfängerin in die zweite Zyklusphase kontrolliert etwa fünf Tage vor dem Embryonentransfer erfolgt.
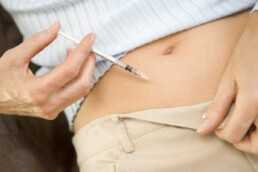
Die einzelnen Schritte für die Spenderin
- Eine Eizellspenderin wird meist im Antagonisten-Protokoll stimuliert, d.h. sie beginnt an Tag zwei ihres Zyklus mit täglichen FSH-Spritzen und spritzt ab Tag fünf oder sechs der FSH-Stimulation zusätzlich einen „Gegenspieler“, damit ihr Eisprung nicht unkontrolliert eintritt. Die Spenderin erhält wie jede andere IVF-Patientin eine genaue Anleitung wie und wann sie sich in die Bauchfalte spritzen muss.
- Die Stimulation dauert ist in der Regel acht bis zehn Tage. Mit Ultraschall wird in diesem Zeitraum ca. zwei Mal die Eizellreifung überprüft.
- Haben die Eizellen die nötige Größe erreicht, wird der Eisprung mit einem Medikament ausgelöst, dass 36 Stunden später die Eizellen löst und gleichzeitig eine Überstimulation verhindert. Da die Empfängerin keinen Embryonentransfer haben wird, geht es bei der Mittelwahl für die Auslösespritze nur um den Schutz der Spenderin. Einnistungsbedingungen können völlig außer Acht gelassen werden.
- Die Eizellentnahme erfolgt unter Kurznarkose und dauert etwa 10 Minuten. Im Aufwachraum wird die Spenderin im Anschluss etwa zwei Stunden medizinisch überwacht.
- Einige Zeit nach der Punktion erfolgt eine gynäkologische Kontrolluntersuchung.
- zwei Wochen später hat die Spenderin dann ihre Blutung und ihr eigener Zyklus beginnt neu.
Seriöse Kinderwunschzentren im Ausland lassen eine junge Frau nicht öfter als drei Mal Eizellen spenden. Jedoch kann die Praxis mangels Meldepflicht nicht ausschließen, dass eine Spenderin in einem anderen Zentrum noch ein viertes oder fünftes Mal spendet.
Ggf. wird die Spenderin durch Abbruch der Stimulation geschützt
Bei allen (jungen wie älteren) Eizellspenderinnen laufen 5-10% aller Zyklen suboptimal. Zum einen kann die Spenderin schlecht auf die Medikamente ansprechen und es wachsen nur wenige Eizellen. Wenn die Empfängerin ihre Synchronisation nicht abbrechen will, greift der behandelnde Arzt dann auf Eizellen aus seiner Eizellbank zurück.
Zum anderen kann eine unvorhergesehene Überstimulation mit über 20 Eizellen passieren. Dann wird die Behandlung zum Schutz der jungen Frau meist abgebrochen. Oftmals greift hier eine soziale Kontrolle durchs Internet, denn kein Kinderwunschzentrum möchte, dass eine junge Spenderin von ihren Beschwerden nach Überstimulation in den einschlägigen Foren schreibt.
Vierzig Jahre nach Geburt des ersten IVF-Kindes ist die IVF-Methode eine hochsichere Behandlung geworden – gleichwohl gibt es Unvorhersehbarkeiten. Dies gilt für Kinderwunschfrauen im eigenen Zyklus ebenso wie für Eizellspenderinnen ohne Embryonentransfer.
Behandlungs-Empfängerin
Eizell-Empfängerin und Eizell-Spenderin werden unterschiedlich auf die bevorstehenden medizinischen Eingriffe vorbereitet. Dabei ist die Behandlung der Empfängerin vergleichsweise einfach. Die aufwendigen Teilschritte – wie Stimulation zur Eizellentnahme und Eizellpunktion – liegen bei der Spenderin.
Bei der Empfängerin gibt es zwei medizinische Ziele
- Verhinderung eines unkontrollierten körpereigenen Eisprungs
- Aufbau der Gebärmutterschleimhaut (Endometrium) auf 7-10/12 mm
Ersteres ist wichtig, da der Eisprung fünf bis sieben Tage später das enge Einnistungsfenster vorgibt. Zum zweiten ermöglicht nur ein gut aufgebautes Endometrium die Einnistung eines entwicklungsfähigen Embryos.

Die Behandlungspläne der Empfängerin variieren leicht, je nachdem ob es sich um einen Frisch- oder um einen Kryotransfer handelt.
Prinzipiell sind Kryotransfers zeitlich für das Kinderwunschzentrum leichter zu steuern. Auch muss bei Frauen nach den Wechseljahren nicht auf den Eisprung geachtet werden, da sie keine Ovulation mehr haben. Letzteres vereinfacht die Planbarkeit der Behandlung für die Klinik.
Vier wesentliche Bausteine der Behandlung der Empfängerin
Die Behandlung orientiert sich an den einzelnen Zyklusphasen. Diese sind
- Zwei bis vier Wochen Einnahme von Östrogentabletten zum sicheren Aufbau des Endometriums.
- Rückmeldung über die Höhe und die Schichtigkeit der Gebärmutterschleimhaut an das ausländische Zentrum. Dazu ist eine Ultraschalluntersuchung notwendig.
- Medikamentöse Unterdrückung der Ovulation der Empfängerin, sofern diese noch vor oder zu Beginn der Wechseljahre ist.
- Übertritt in die zweite Zyklushälfte durch die Einnahme bzw. durch vaginales Einführen von Progesteronpräparaten.
Besonderheiten bei Empfängerinnen vor der Menopause
Bei einem Frischzyklus der Empfängerin vor der Menopause erfolgt eine Downregulation und eine kontinuierliche Gabe von Östrogen. Der körpereigene Eisprung wird unterdrückt.
Bekommt die Spenderin die Auslösespritze oder Punktion, nimmt die Empfängerin ab dem Zeitpunkt Progesteron ein.
Die Empfängerin wird damit empfängnisbereit gehalten und wartet sozusagen auf die Spenderin. Es gibt einen relativ großen zeitlichen Spielraum wie lange die Empfängerin in der ersten Zyklusphase bleiben kann. Entscheidend wichtig ist, dass beide Frauen zeitgleich in die zweite Zyklusphase übertreten.
Fresh or frozen?
Im Vorfeld der Eizellspende beschäftigen sich Kinderwunschpaare mit vielen wichtigen Detailfragen. Eine wesentliche Entscheidung nach der anderen muss gefällt werden. Vor allem diejenige, ob sie besser Eizellen aus einer frischen Stimulation der Spenderin verwenden oder kryokonservierte aus einer Eizellbank.
Auswertungen der Ergebnisse von großen IVF-Zentren mit Top-Laboren im Ausland, die sowohl mit Frischzyklen als auch mit kryokonservierten Spendereizellen arbeiten, zeigen: Bei beiden Verfahren ist die Schwangerschaftsrate in IVF-Zentren vergleichbar positiv.
Beide Methoden haben Vor- und Nachteile, so dass sich die Empfängerpaare an persönlichen Präferenzen orientieren müssen.

Die Methode des Frischzykluses
- Die Herkunft der Eizellen ist transparenter. Fünf Tage vor dem Embryonentransfer an eine Empfängerin wurde hier vor Ort eine Spenderin punktiert. Es sind im Regelfall keine „internationalen Spenderinnen“ bzw. Eizellen mit unbekannter Herkunft. Einem möglichen „Eizell-Shipping“ quer durch Welt wird kein Vorschub geleistet.
- Im bestmöglichen Fall erhält die Empfängerin bei Frischzyklen 10-12 Eizellen – je nach „Verteilungspolitik“ des Zentrums und Modellwahl des Paares (z.B. innerhalb eines Premiumpaketes). Es gibt einige Frauen, die daraus drei Kinder nacheinander bekommen haben. Diese Kinder sind dann genetisch 100% miteinander verwandt.
- Ein evtl. doppeltes Einfrieren wird vermieden. Zuerst war die Eizelle tiefgefroren, dann werden womöglich überzählige Blastozysten kryokonserviert.
- Es gibt noch keine Langzeituntersuchungen ob Vitrifikation einen langfristigen Einfluss auf die Genexpression des daraus entstehenden Menschen hat. Aktuell gibt es keine Hinweise dafür. Qualifizierte Aussagen darüber sind unmöglich, denn dazu ist die circa achtzehnjährige Methode noch zu jung.
Die Methode eines Zykluses mit kryokonservierten Eizellen
- Die Auswahl an Spenderinnen ist größer. Das Matching kann insbesondere in IVF-Zentren mit großen Eizellbanken relativ differenziert erfolgen.
- 10% aller Spenderinnen reagieren unerwartet suboptimal auf die Stimulation. Zu wenig Eizellen, mangelhafte Qualität und Reife etc. Für das Empfängerpaar ist das sehr enttäuschend.Auch kann es zu einem Abbruch des Zykluses der Empfängerin kommen. Sind die Zellen jedoch tiefgefroren, ist dieses Problem nahezu ausgeschlossen. Die Anzahl der Eizellen, die mit dem Sperma des Partners befruchtet werden und in die Kultur gehen, ist planbar. Eingefroren werden nur reife Oozyten in Metaphase zwei.
- Eizellen sind eine wertvolle Ressource. Wenn eine Empfängerin bereits im ersten Zyklus mit der ersten Blastozyste schwanger wird, wurden Eizellen gespart, die dann anderen Frauen zur Verfügung stehen. Überzählige und verwaisende Embryonen werden vermieden.
- Der Zeitpunkt für den Embryonentransfer ist auf den Tag genau planbar. Dabei wird die Empfängerin empfängnisbereit gehalten und kurz vor oder am Tag des Auftauens mit Progesterongaben in die zweite Zyklusphase gebracht. So wird Stress für die Empfängerin vermieden und das IVF-Zentrum hat geregelte Arbeitszeiten.
Wie funktioniert Vitrifikation?
Genaues Hintergrundwissen wie Vitrifikation funktioniert.
Einfrieren von Spermien
Genaues Hintergrundwissen wie slow freezing funktioniert.
„Ich bevorzuge tendenziell die Spende im Frischzyklus aus zwei Gründen:
1. Die Spenderin kommt aus der Stadt bzw. der Gegend, in dem das IVF-Zentrum liegt (Transparenz)
2. Ich vermeide gern ein doppeltes Einfrieren – erst die Eizelle und dann evtl. überzählige Embryonen
Allerdings kann für Paare mit großem Sicherheitsbedürfnis oder mit traumatischen Vorerfahrungen on der Reproduktionsmedizin ein Zyklus mit kryokonservierten Eizellen indizierter sein.“
– Christine Büchl
Genetische Tests
Grundsätzlich können human-genetische Untersuchungen sowohl beim Kinderwunschpaar, bei der Eizellspenderin und/oder beim Embryo durchgeführt werden.
Soll ein Test beim Embryo (Präimplantationsdiagnostik) gemacht werden, braucht es in Deutschland -die Zustimmung der Ethikkommission. Im Ausland gehören genetische Tests von Embryonen teilweise zur Routine oder sind eine optionale Zusatzleistung.
Es lassen sich zwei Arten von Tests unterscheiden:
- Karyogramm
Dabei werden alle 23 Chromosomenpaare numerisch überprüft. Insbesondere Trisomien und Transloskationen können so erkannt werden.

- Next Generation Sequencing (NGS-Tests)
Die Multi-Gen-Panels für diese Diagnostik werden Jahr für Jahr schneller und kosteneffizienter. Sie identifizieren mittlerweile ca. 1600 krankheitsrelevante Gene (Stand November 2021). Ein Gen zu erkennen, bedeutet noch nicht, dass die Krankheit im Laufe des Lebens ausbricht. Viele der so identifizierbaren Krankheiten sind therapierbar bzw. symptomatisch in Griff zu bekommen.
Statistisch belegbar ist, dass viele gesunde und unauffällige Personen, die sich einem NGS-Test unterziehen, „Treffer“ diagnostiziert bekommen. Bedeutet: Die Person ist rezessiver Träger einer oder mehrerer Erkrankungen. Sie ist selbst nicht erkrankt, gibt jedoch die Einschränkung eventuell an ihre Nachkommen weiter.
Damit eine der testbaren Krankheiten zum Ausbruch kommt, müssen Mann und Spenderin denselben Gendefekt haben. Nach der Mendelschen Vererbungsregel ist dann die Erkrankung in 25% aller Fälle dominant, sprich es entwickelt sich das volle Krankheitsbild. Wie schlimm die Krankheit ist, ist individuell-persönlich oder medizinisch einzuordnen.
Viele Kliniken, die Eizellspenden anbieten, haben NGS-Tests für die Spenderin und den Mann als Wahlleistung im Angebot. Die Kosten belaufen sich je nach Land auf 800 bis 1.500 Euro pro Person.
Diese Optimierung der Fortpflanzungsmedizin bringt folgenreiche Veränderungen: Die Eizellen einer NGS- sequenzierten Spenderin werden mittlerweile als „höherwertig“ angesehen und verkaufen sich besser. Die Vor- und Nachteile einer Diagnostik sowie ethischen Fragen muss jeder individuell für sich beantworten.
Bei Babys und Kleinkindern mit unklaren Auffälligkeiten und Entwicklungsverzögerungen haben NGS-Tests heute einen hohen diagnostischen Stellenwert. Sie können Familien in der Ursachenfindung entlasten.
Matching
Matching ist die Zuordnung einer Spenderin zu einer Empfängerin. Damit das mögliche Kind phänotypisch in die Familie passt werden dabei bestimmte Merkmale abgeglichen.
Welche Merkmale werden herangezogen?
- Augenfarbe
- Haarfarbe – und struktur
- Ungefähre Größe
- Körperbau
- Blutgruppe
Diese Matching-Kriterien sind internationaler Standard und keine extra Leistung einzelner Kliniken.

Diese Matching-Kriterien sind internationaler Standard und keine extra Leistung einzelner Kliniken.
Wenn nicht anders gewünscht, orientiert sich das Kinderwunschzentrum beim Matching an den äußeren Merkmalen der Empfängerin. Dazu füllt das Kinderwunschpaar beim Erstgespräch oder beim Abschluss des Behandlungsvertrages eine Liste mit den Merkmalen beider Partner aus. Diese ist dann Arbeitsgrundlage für die Suche nach einer geeigneten Spenderin bzw. für die Auswahl der Eizellen.
Ist es schwierig eine passende Spenderin zu finden, z.B. weil die Empfängerin sehr hellhäutig ist, grüne Augen und rote Locken hat, kann auch auf den Ehemann ausgewichen werden und eine Spenderin nach seinem Aussehen ausgewählt werden.
Feinmerkmale wie die Formen von Ohren, Hände und Lippen werden hingegen kaum berücksichtigt. Dies würde vor allem bei einer Frischspende den Kreis der in Frage kommenden Spenderinnen zu sehr einschränken.
Beim Matching geht es nicht um Miniversion der Empfängerin, sonderndarum, eine ungefähr ähnlich aussehende Spenderin zu finden. Fotos des Paares sind dabei hilfreich und dienen zur Orientierung. Doch hier gilt es vorsichtig mit der Erwartungshaltung umzugehen: Der Stellenwert von Fotos wird von vielen Empfängerpaaren überinterpretiert. Computergestütze Bilderkennungsprogramme für das Matching werben mit einer hohen Ähnlichkeit zwischen Spenderin und Empfängerin. Sie setzen eine große Eizellbank voraus.
Viele Experten halten Kriterien wie Alter der Spenderin, Anzahl und Qualität der Eizellen für weit wichtiger als eine genaue phänotypische Ähnlichkeit.
Die Sache mit der Blutgruppe
Hier kommt es häufig zu einem Missverständnis zwischen Paar und Klinik. Die Blutgruppe zwischen Empfängerin und Spenderin muss nur übereinstimmen wenn das Paar plant, das Kind nicht aufzuklären. Die Blutgruppe des Kindes ist nicht relevant für den Schwangerschaftsverlauf. Letzteres ist nur wichtig, bei einer fehlenden Kompatibilität des Rhesusfaktors in einer zweiten Schwangerschaft.
Anders herum erklärt: Eine Frau mit der Blutgruppe A positiv wird mit eigenen Eizellen schwanger von einem Mann mit der Blutgruppe B positiv. Das Kind hat die Blutgruppe B positiv geerbt und wächst im Körper der A positiven Frau heran. Daraus entstehen weder für die Mutter noch für das Kind medizinische Probleme.
Dass der Blutgruppe im Matching eine große Bedeutung zugewiesen wird ist historisch gewachsen und stammt aus Zeiten als die Nicht-Aufklärung des Kindes empfohlen wurde. Schließlich sollte das Kind später im Biologieunterricht nicht feststellen müssen, das es bspw. mit seiner B negativen Blutgruppe gar nicht zu seinen Eltern passen kann die beide A positiv sind.
Paare, denen äußere Merkmale für das Matching nicht wichtig sind
Paare können dem ausländischen Kinderwunschzentrum sagen, dass sie keinen Wert auf die Übereinstimmung von äußeren Merkmalen und/oder Blutgruppe legen. Dies erweitert bei einer Frischspende den Kreis der möglichen Spenderinnen. Besonders geeignet ist dies für Partner, die untereinander sehr unterschiedlich aussehen, und die sicher vorhaben, das Kind aufzuklären. Die Hautfarbe sollte jedoch gleich sein und zum Wohle des möglichen Kindes nicht zur Disposition stehen.
Idealtypischer Ablauf einer Eizellspende
Wann läuft es wirklich gut? Was darf das Empfängerpaar von der Behandlung im Ausland erwarten?
Kinderwunschpaare die sich für eine Eizellspende entscheiden sind leidgeprüft und an schlechte Ergebnisse gewöhnt.
So ist es nicht leicht zu verstehen, dass bei einer Spenderbehandlung andere Gesetzmäßigkeiten gelten. Wer gerne mehr als ein Kind plant, sollte mit allen Eizellen aus einer Stimulation der Spenderin starten.

Idealtypischer Verlauf eines Frischzyklus (alle Eizellen für eine Empfängerin)
Idealtypischer Verlauf eines Frischzyklus mit vertraglich begrenzter Eizellanzahl („Basisprogramm“)
Idealtypischer Verlauf eines Zyklus mit Zellen aus der Eizellbank
1,2 oder 3?
Die Zwillingsrate beträgt nach Eizellspende über 30%, die Drillingsrate liegt bei 6%.
Eine Reihe von IVF-Zentren transferieren einer Frau über 45 auf Grund von gesundheitlichen Risiken im Falle einer Schwangerschaft keine zwei Embryonen. Dieser Cut off ab einem gewissen Alter steht in diesen Zentren nicht zur Diskussion.
Die Frage, ob ein oder zwei Embryonen transferiert werden sollen, ist nicht einfach zu beantworten.

Für viele Paare sprechen bei der Eizellspende gute Gründe für den Transfer von zwei Embryonen:
- Höhere Erfolgswahrscheinlichkeit. Kinderwunschpaare sind oft derart am Limit, dass sie den schnellen Erfolg suchen.
- weniger Anreisen in das ausländische IVF-Zentrum
- Kostenersparnis, da jeder Kryotransfer ca. 800.- – 1500.-€ kostet
- Für ein potentielles geplantes Geschwisterkind zwei Jahre später wäre man dann fast schon zu alt
- Die Familienplanung kann nach der Geburt von zwei Kindern endlich abgeschlossen werden
- Die doppelte Fruchtbarkeit ist eine Art innerer Belohnung nach Jahren der Sterilität
Immer mehr Reproduktionsmediziner im In- und Ausland können mit einem gewünschten single embryo transfer gut mitgehen:
- weniger Schwangerschaftskomplikationen; insbesondere auch die zwillingstypischen
- Besserer gesundheitlicher Zustand des Kindes nach einer Einlingsschwangerschaft (sog. „outcome“)
- Single embryo transfers führen genauso zu Schwangerschaften, da die Embryonen dieselben sind. Nur wird ein Embryo nach dem anderen transferiert und damit ist mehr Ausdauer des Paares gefordert.
- Weniger Belastung und ungünstige Familienentwicklung in den ersten Lebensjahren des Kindes
Für die meisten Paare befürworte ich einen single embryo transfer- insbesondere bei einer AA-Blastozyste. Überspitzt gesagt: Was man bei einem Transfer von zwei Embryonen weniger ins Ausland fährt, fährt man später mit den beiden mehr zum Kinderarzt, zu Ergo- und sonstigen Therapeuten.
– Christine Büchl
Für den Reproduktionsmediziner ist es eine Arbeitserleichterung, wenn Paare bereits mit einer klaren Einstellung kommen, ob sie den Transfer von ein oder zwei Embryonen möchten. Dieser Wunsch des Paares wird in guten IVF-Zentren respektiert. Die Mehrzahl der Paare entscheidet sich für zwei Embryonen, jedoch gibt es wie im homologen IVF auch einen deutlichen Trend hin zum Trasnfer eines Embryos.
Vom Transfer von drei Embryonen bei Eizellspende ist und ohne Wenn und Aber abzuraten, da das Drillingsrisiko bei etwa 6% liegt.
Hier einige Hintergrundinformationen über Drillingsschwangerschaften:
- Die Kinder kommen durchschnittlich sieben Wochen zu früh per Kaiserschnitt auf die Welt.
- Jede 10. Drillingsschwangerschaft endet auf Grund von unaufhaltbaren Frühgeburtsbestrebungen aber schon wesentlich früher, z.B. in der 26. Woche (Geburtsgewicht jedes Kindes dann ca. 800g)
- (Extreme) Frühgeburtlichkeit hat gesundheitliche Folgeproblematiken für die Kinder: Augenschäden, Lungenprobleme, Infektanfälligkeit, Entwicklungsverzögerung etc. Bei sehr schwierigen Verläufen nach Frühgeburtlichkeit kann es auch zu Behinderungen kommen.
- Die Familienentwicklung ist in den meisten Fällen ungünstig, da chronische Überlastung, dauernde Arzt- und Therapietermine die Eltern völlig überfordern und die Paarbeziehung schwer belasten.
„Ich habe in den letzten Jahren drei höhergradige Mehrlingsschwangerschaften nach Eizellspende mitbetreut. Alle drei Eizellspenden wurden außerhalb der EU durchgeführt. Hohe Erfolgsrate, notfalls Reduktion von überzähligen Feten, war die medizinische Linie der IVF-Zentren. Alle Paare waren aus meiner Sicht sehr schlecht beraten worden. Zwei der drei Paare entschieden sich für einen selektiven Fetozid in der Schwangerschaft. Vom Kinderwunsch direkt in den Schwangerschaftskonflikt katapultiert zu werden, ist psychisch einer der tiefsten Punkte, an denen ein Paar ankommen kann.“
– Christine Büchl
Risiken
„…Die Risiken für Bluthochdruck, Präeklampsie, geringes Geburtsgewicht, Frühgeburt, Kaiserschnitt und Blutungen nach der Geburt sind bei Eizellspenden verglichen mit IVF- oder Spontanschwangerschaften erhöht…“
„ …Weil einige Risiken von Schwangerschaften nach einer Eizellspende, wie z.B. Bluthochdruck und Blutungen nach der Geburt bei Mehrlingen erhöht sind, soll ein Single Embryo Transfer (SET) empfohlen werden…“
„…Die Wahrscheinlichkeit eine Schwangerschaftsdiabetes zu entwickeln ist bei Eizellspende nicht erhöht…“
So fasst eine der größten Metaanalysen aus dem Jahr 2016 die Risiken einer Eizellspendenschwangerschaft zusammen. (Storgaard, Pinborg, 2017 -1*)

In der Studie wurden 21 Einzelstudien mit 11.000 Schwangerschaften nach Eizellspende, 118.000 IVF/ICSI Schwangerschaften und 1 Million Spontanschwangerschaften ausgewertet.
Frühgeburt wird dabei als Geburt vor der 37. Schwangerschaftswoche definiert und von Bluthochdruck spricht man bei Werten über 140/90.
Die unten genannten Risiken und Komplikationen sind nach einer Eizellspende durchschnittlich um das Zwei- bis Dreifache erhöht.
Wahrscheinlichkeit von Komplikationen
Folgende Häufigkeiten pro 100 Schwangere wurden in den 21 Einzelstudien herausgefunden:
| Eizellspende | Homologer IVF / ICSI | Spontankonzeption | |
| Präeklamsie | 9,3 – 16,9% | 3,2 – 11,5 % | 2,4 – 3,8% |
| Bluthochdruck |
13,0 -39,3% |
1,9 – 23,3% | 2,1 – 3,8% |
| Kaiserschnitt (Einling) | 31,4 – 81,0% | 25,3 – 56,0 % | 16,3 – 17,5 % |
| Frühgeburt (Einling) | 10,0 – 24,3 % | 13,3 – 13,4 % | 4,4 – 5,0% |
Für den Laien ist überraschend, dass sich die 21 Einzelstudien untereinander sehr in ihrer Spannbreite unterscheiden.
Bei Zwillingsschwangerschaften nach Eizellspende steigen die Komplikationen signifikant: Bluthochdruck wird in 23,8 – 62,5 % aller Fälle und Präeklampsie in 15,8 – 45,8 % aller Fälle dokumentiert.
Bei der Kaiserschnittrate vermuten auch die Autoren der o.g. dänischen Studie eine hohe Anzahl an Wunschkaiserschnitten.
Auch eine 2021 erschienene Studie von Berliner Medizinern kam auf ähnliche Ergebnisse. Bei den untersuchten 115 Schwangerschaften nach Eizellespende kam es in 16% der Einlings- und in 23% der Zwillingsschwangerschaften zu einer Präeklampsie. Die Einlinge wurden durchschnittlich in der 35. Schwangerschaftswoche entbunden, die Zwillinge in der 34. Woche. Die Kaiserschnittrate lag bei weit über 80%. 2)
1) M Storgaard, A Pinborg et al.,PubMed 2017 Mar; 124(49): 561-572
2) Altmann, J.Kummer, F.Herse, L.Hellmeyer, D.Schlembach, W.Henrich, A.WeichertPubMed 2021 Oct, 0.1007/s00404-021-06264-8
Fragestellungen an sich selbst und an den Gynäkologen des Vertrauens
Diese weltweit größte Metaanalyse von Schwangerschaften nach Eizellspende gibt Kinderwunschpaaren ein umfangreiches Datenmaterial an die Hand.
Die Anschlussfragen für Kinderwunschpaare lauten daher:
- Welches Risiko sind wir bereit einzugehen?
- Wie sind auftretende Probleme medizinisch in Griff zu bekommen?
- Wie oft tritt wirklich eine sehr schwere Komplikation ein (HELLP Syndrom, Geburt vor der 28. SSW)?
Diese sollten Sie im Vorfeld mit den deutschen Medizinern Ihres Vertrauens diskutieren. Die ausländischen Kliniken verfolgen meist die Schwangerschaft nicht detailliert nach. Sehr schwere Verläufe und Komplikationen sind zum Glück selten.
Transparent informieren und offen kommunizieren
Nichtsdestotrotz wäre es keine gute Idee, den die Schwangerschaft betreuenden Gynäkologen und den Pränatalmediziner nicht über die erfolgte Eizellspende zu informieren. Nur wenn die Mediziner Bescheid wissen, können sie verlässlich erweiterte Risikoprofile und einen engmaschigen spezifischeren und notwendigen Überwachungsbedarf ausmachen.
Gut für Sie zu wissen ist auch, dass in Deutschland ab dem Zeitpunkt des positiven Schwangerschaftstests Ihre Ärzte und Beraterinnen juristisch „safe“ sind. Juristische Gradwanderungen gibt es für diese Berufsgruppen nur vor und während der Eizellspendenbehandlung.
In einer weiteren Veröffentlichung zu ihrer großen Metaanalyse meinen die o.g. dänischen Autoren „….Die Empfehlungen sollten Single Embryo Transfer beinhalten und Betreuung in einer hochspezialisierten Unit vor und während der Geburt“ (Storgaard, Pinborg, 2017).
„Die wahre Qualität eines Kinderwunschzentrums zeigt sich nicht in der Schwangerschaftsrate als solcher, sondern in der Schwangerschaftsrate in Relation zur durchschnittlichen Anzahl der transferierten Embryonen. Eine hohe Schwangerschaftsrate darf nicht mit einer hohen Zwillingsrate „erkauft“ werden.
60% Schwangerschaftsrate bei 1,1 durchschnittlich transferierten Embryonen ist top; 60 % bei 2,2 transferierten Embryonen ist kein sonderliches Kunststück.“
– Christine Büchl
Schwangerschaft
„Der Mann ist mit drinnen und die Frau liebt das Kind sowieso“ so pragmatisch urteilen Reproduktionsmediziner über die Eizellspende. Die Frau hat die Bindung an das Kind durch die Schwangerschaft, der Mann ist genetischer und sozialer Vater.
Die Hormonumstellung, das einzigartige Körpergefühl in der Schwangerschaft und die Überwindung der langen Jahre der Kinderlosigkeit, erzeugen Bindung bei Frau.
Der Körper unterscheidet nicht dass es sich um eine fremde Eizelle handelt. Das physische und psychische Schwangerschaftsprogramm läuft an. Es endet mit der Geburt.

Schwangerschaftsrate nach Behandlung mit Eizellspende

Diese Erfolgszahlen sind ECHT.
Abortrate
Die Wahrscheinlichkeit das Kind wieder zu verlieren – die sog. Abortrate – beträgt nach Eizellspende 10-15 Prozent. Im Vergleich dazu hat eine Frau Anfang bis Mitte 40, die mit eigenen Eizellen und nach einer IVF-Behandlung schwanger wird, ein durchschnittliches Risiko von 40 bis 65 Prozent, das Kind wieder zu verlieren. Nach Eizellspende hat eine Frau über 40 das Abgangsrisiko einer Frau, die zehn bis 15 Jahre jünger ist.

Medizinische Versorgung in der Schwangerschaft
Sollten in einer Schwangerschaft nach Eizellspende Komplikationen auftreten, dann sind sie in aller Regel nicht genetischer und auch nicht geburtshilflicher Natur. Das Erste tritt wegen des jungen Eizellalters nicht ein und das Zweite ergibt sich aus der Erfahrung, dass Kinderwunschpaare nicht zögern, beim geringsten Risiko einem Kaiserschnitt zuzustimmen. Es besteht ein moderates Risiko der Frühgeburtlichkeit des Kindes wenn die Mutter Präeklampsie in der Schwangerschaft entwickelt.
Zum eigenen Schutz und für das Wohlergehen des Ungeborenen ist es unabdingbar, den behandelnden Gynäkologen die Entstehungsgeschichte des Kindes zu erzählen. Er hat das Präeklamsie-Risiko auf dem Schirm. Die Eizellspendenschwangere wird dann intensiver betreut. Vorteilhaft ist es auch, sich prophylaktisch von einem Pränatal-Zentrum mitbetreuen zu lassen. Die Ärzte dort haben schon Hunderte von Schwangerschaften nach Eizellspende überwacht.
Die Schwangerschaft nach erfolgreicher Eizellspende zu betreuen, stellt für Ärzte und Berater kein juristisches Risiko dar. Das deutsche Embryonenschutzgesetz verbietet die Beihilfe nur vor einer Behandlung mit Eizellspende. Auch für die Krankenkassen ist die Schwangerschaft nach Eizellspende wie jede andere Schwangerschaft auch. Es besteht voller Leistungsumfang.
Für die Entbindung ist ein Krankenhaus mit der maximalen Versorgungsstufe empfehlenswert.
Aufregung in der Frühschwangerschaft
Schwangerschaften nach langer Kinderwunschzeit sind zu Beginn immer Angstschwangerschaften. Das Kontroll- und Sicherheitsbedürfnis der Schwangeren, die noch nichts oder nichts mehr spürt, ist überbordend.
Ärztlich feststellbar ist eine intakte Schwangerschaft ist wie folgt:

Wichtig: Der Progesteronwert ist zu Beginn einer Eizellspendenschwangerschaft naturgemäß sehr niedrig. Progesteron wird nicht körpereigen gebildet sondern über Vaginaltabletten und / oder Spritzen extern zugeführt. Diese Medikamente gehen kaum ins Blut über und sind bei einer Blutentnahme nicht nachweisbar.
Viele Gynäkologen wissen dies nicht und es entsteht unnötige Panik bei der Frau. Die sichere Einschätzung des Progesteronwertes überlässt das Paar besser dem ausländischen IVF-Zentrum.
Sehr hohe psychologische Bedeutung hat später das Stillen des Kindes. Endlich etwas, was funktioniert. Schwierigkeiten beim Stillen – und diese hat jede Erstgebärende – erfordern eine engmaschige Stillberatung damit die frischgebackene Mutter nicht vorzeitig aufgibt.
